乔默生物技术(上海)有限公司品牌商
5 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0.6000000000000001
- 0.6000000000000001
- 2.6
- 2.6
anti-Mouse CD3 Purified,17A2 Clone,Functional assay
¥1350
推荐产品
新冠蛋白SARS-CoV-2 Nucleocapsid Protein (Omicron B1.1.529 Variant), Tag Free, HEK293
品牌:Chamot Biotech/乔默生物
¥5400
咨询公司新闻/正文
不同来源的巨噬细胞极化诱导操作指南(三)
1828 人阅读发布时间:2024-02-22 14:56
THP-1细胞是从急性单核细胞白血病患者的外周血中分离得到的单核细胞系,为悬浮细胞,它在调控组织稳态、炎症反应等方面的研究发挥着重要作用,该细胞株已被广泛用于研究单核/巨噬细胞的功能机制、信号通路、营养和药物转运、免疫应答等方面。相对于人外周血单核细胞(PBMC),THP-1更易在实验室中培养和扩增,且具有更稳定的基因背景,不存在PBMC的个体差异性问题,利于实验结果的重现。
RAW264.7细胞是小鼠单核巨噬细胞白血病细胞,为贴壁细胞,是从用Abelson鼠科白血病病毒诱导的雄性小鼠的肿瘤中建立的单核/巨噬样细胞系。RAW264.7细胞是破骨细胞、炎症研究最常用的体外模型之一。
巨噬细胞是免疫系统中的重要组成部分,在保护机体免受感染和维持组织平衡方面等发挥着关键作用。 为了更便利地研究巨噬细胞的功能和机制,科学工作者们创造了一种不需要从患者或动物采集组织的方法,即是选择商业化的人和小鼠单核细胞系,如THP-1细胞(急性单核细胞白血病)、RAW264.7细胞(小鼠白血病单核巨噬细胞)等。
一、THP-1细胞来源巨噬细胞极化及鉴定
1.1 用RPMI 1640完全培养基(1640培养基+10%FBS+双抗)重悬细胞至2-10×10^5/ml,加入终浓度为100ng/ml的PMA,24孔培养板中加入1ml细胞悬液,诱导分化24h,替换成新鲜RPMI 1640完全培养基,继续培养24h。
1.2 M1方向极化:加入10ng/ml的LPS和20ng/ml的Human IFN-γ,极化24h;
1.3 M2方向极化:加入20ng/ml的Human IL-4和20 ng/ml的Human IL-13,极化24h;
1.4 细胞鉴定:通过qRT-PCR、ELISA、流式细胞术等方法进行鉴定。(M1标记物如:CD80, iNOS, IL-1β, IL-6, CXCL1等;M2标记物如 CD206, CD163, IL-10, CCL18,Arg1等)
二、RAW264.7细胞来源巨噬细胞极化及鉴定
2.1 用DMEM完全培养基(DMEM培养基+10%FBS+双抗)重悬细胞至2-10×10^5/ml,24孔培养板中加入1ml细胞悬液,培养过夜。
2.2 M1方向极化:加入10ng/ml的LPS和20ng/ml的Mouse IFN-γ,极化24h;
2.3 M2方向极化:加入20ng/ml的Mouse IL-4,极化24h;
2.4. 细胞鉴定:通过流式细胞术、ELISA、qRT-PCR等方法进行鉴定。(M1标记物如:CD80, iNOS, IL-1β, IL-6, CXCL1等;M2标记物如 CD206, CD163, IL-10, CCL18,Ar1g1等)
*以上流程仅供参考,具体实验需跟情况做调整。
所需细胞因子:
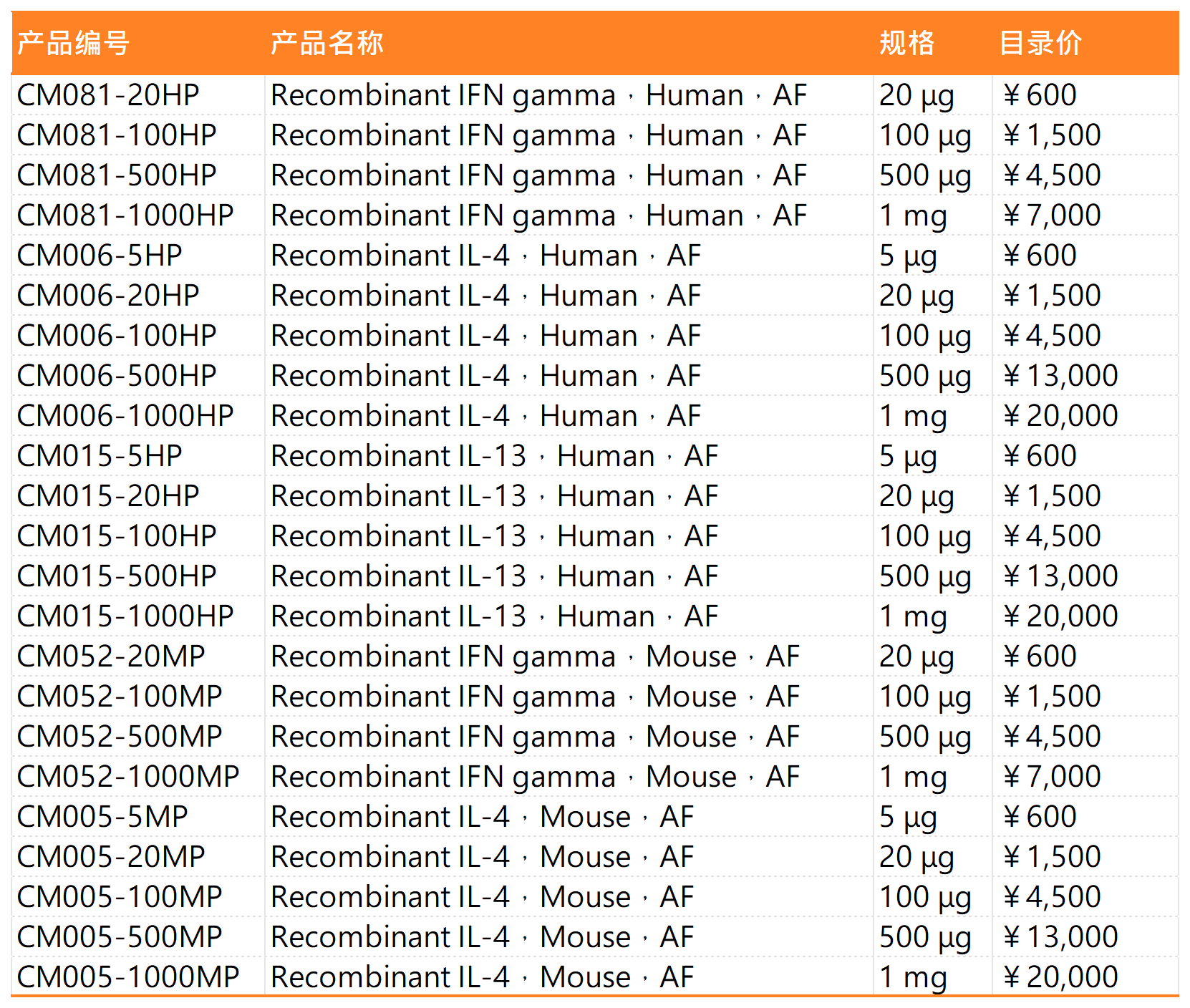
参考文献
RAW264.7细胞是小鼠单核巨噬细胞白血病细胞,为贴壁细胞,是从用Abelson鼠科白血病病毒诱导的雄性小鼠的肿瘤中建立的单核/巨噬样细胞系。RAW264.7细胞是破骨细胞、炎症研究最常用的体外模型之一。
巨噬细胞是免疫系统中的重要组成部分,在保护机体免受感染和维持组织平衡方面等发挥着关键作用。 为了更便利地研究巨噬细胞的功能和机制,科学工作者们创造了一种不需要从患者或动物采集组织的方法,即是选择商业化的人和小鼠单核细胞系,如THP-1细胞(急性单核细胞白血病)、RAW264.7细胞(小鼠白血病单核巨噬细胞)等。
一、THP-1细胞来源巨噬细胞极化及鉴定
1.1 用RPMI 1640完全培养基(1640培养基+10%FBS+双抗)重悬细胞至2-10×10^5/ml,加入终浓度为100ng/ml的PMA,24孔培养板中加入1ml细胞悬液,诱导分化24h,替换成新鲜RPMI 1640完全培养基,继续培养24h。
1.2 M1方向极化:加入10ng/ml的LPS和20ng/ml的Human IFN-γ,极化24h;
1.3 M2方向极化:加入20ng/ml的Human IL-4和20 ng/ml的Human IL-13,极化24h;
1.4 细胞鉴定:通过qRT-PCR、ELISA、流式细胞术等方法进行鉴定。(M1标记物如:CD80, iNOS, IL-1β, IL-6, CXCL1等;M2标记物如 CD206, CD163, IL-10, CCL18,Arg1等)
二、RAW264.7细胞来源巨噬细胞极化及鉴定
2.1 用DMEM完全培养基(DMEM培养基+10%FBS+双抗)重悬细胞至2-10×10^5/ml,24孔培养板中加入1ml细胞悬液,培养过夜。
2.2 M1方向极化:加入10ng/ml的LPS和20ng/ml的Mouse IFN-γ,极化24h;
2.3 M2方向极化:加入20ng/ml的Mouse IL-4,极化24h;
2.4. 细胞鉴定:通过流式细胞术、ELISA、qRT-PCR等方法进行鉴定。(M1标记物如:CD80, iNOS, IL-1β, IL-6, CXCL1等;M2标记物如 CD206, CD163, IL-10, CCL18,Ar1g1等)
*以上流程仅供参考,具体实验需跟情况做调整。
所需细胞因子:

参考文献
- Marie Genin, Francois Clement, Antoine Fattaccioli, etc. M1 and M2 macrophages derived from THP-1 cells differentially modulate the response of cancer cells to etoposide.BMC Cancer. 2015 Aug 8:15:577.
- Xuan Huang, Yong Li, Mingui Fu, etc. Polarizing Macrophages In Vitro.Methods Mol Biol. 2018:1784:119-126.
- Ingrid Elisia, Han Bee Pae, Vivian Lam, etc. Comparison of RAW264.7, human whole blood and PBMC assays to screen for immunomodulators.J Immunol Methods. 2018 Jan:452:26-31.
- Hiromi Shiratori, Carmen Feinweber, Sonja Luckhardt, etc. THP-1 and human peripheral blood mononuclear cell-derived macrophages differ in their capacity to polarize in vitro. Mol Immunol. 2017 Aug:88:58-68.
- F Kianoush, M Nematollahi, J D Waterfield, etc. Regulation of RAW264.7 macrophage polarization on smooth and rough surface topographies by galectin-3. J Biomed Mater Res A. 2017 Sep;105(9):2499-2509.
- E W Baxter, A E Graham, N A Re, I M Carr, etc. Standardized protocols for differentiation of THP-1 cells to macrophages with distinct M(IFNγ+LPS), M(IL-4) and M(IL-10) phenotypes. J Immunol Methods. 2020 Mar:478:112721.