乔默生物技术(上海)有限公司品牌商
5 年
手机商铺
- NaN
- 0.6000000000000001
- 0.6000000000000001
- 2.6
- 2.6
推荐产品
新冠蛋白SARS-CoV-2 Nucleocapsid Protein (Omicron B1.1.529 Variant), Tag Free, HEK293
品牌:Chamot Biotech/乔默生物
¥5400
咨询公司新闻/正文
IL-12在肿瘤免疫治疗中的应用
870 人阅读发布时间:2024-07-05 10:09
白介素12(Interleukin-12, IL-12)是IL-12家族的一员,IL-12家族细胞因子是一组独特的异二聚体细胞因子,包括IL-12、IL-23、IL-27、IL-35和IL-39。有研究从效应免疫功能和调节免疫功能方面证实了IL-12家族细胞因子在癌症形成先天和适应性免疫反应中的重要性,并确定了不同IL-12家族成员的多重作用。这些细胞因子可作为开发免疫调节治疗方法的有希望的候选者。IL-12由α亚基(p40)和β亚基(p35)亚基组成的70kDa的异二聚体细胞因子,被认为是一种主要的促炎细胞因子。α亚基(IL12p35)与IL-6具有序列同源性,也可以是IL-23(p19–p40)的一部分,而β亚基(IL12p40)与IL-35(p35/Ebi3)共享。
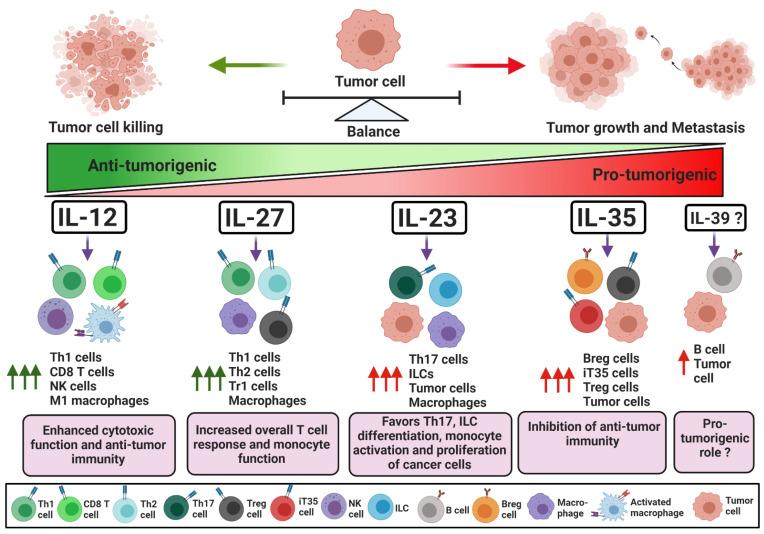
图 IL-12家族细胞因子在肿瘤发生中维持效应免疫反应和调节免疫反应之间平衡的作用
(源自Cancers (Basel). 2021 Jan; 13(2): 167)
IL-12主要由活化的抗原呈递细胞如DC、巨噬细胞、单核细胞和B细胞产生。IL-12的产生是一个严格控制的过程,主要在转录水平上受到调控,通过在感测病原体相关分子模式时激活病原体识别受体(例如抗原呈递细胞中的Toll样受体)或损伤相关分子模式来启动产生。此外,细胞因子刺激和直接免疫细胞-细胞接触,包括CD40-CD40L相互作用,也会诱导IL-12的产生。后一种CD40依赖性机制可能是癌症产生IL-12的主要机制。IL-12与IL-12受体(IL-12R)结合,IL-12R受体主要在T细胞和NK细胞上表达,为IL-12Rβ1和IL-12Rβ2亚基组成的高亲和力异源二聚体。β1亚基在免疫细胞上组成性表达,而β2亚基在激活后在T细胞和NK细胞中上调。
IL-12R的激活导致激酶Janus激酶(JAK2)和Tyk2的募集,以及随后信号转导子和转录激活子4(STAT4)的磷酸化。磷酸化STAT4的二聚和核转位最终导致IFN-γ的产生、CD4+和CD8+T细胞向I型辅助T细胞(Th1)分化的转录重编程和NK细胞的成熟。IFN-γ导致FAS配体依赖性髓系室的崩溃和M1巨噬细胞极化,为最佳的T细胞浸润和细胞溶解功能铺平了道路。此外,IL-12的强大抗血管生成特性也使其成为癌症治疗的有吸引力的细胞因子。抗血管生成作用是由IFN-γ的产生介导的,IFN-γ改变了细胞外基质的重塑和内皮细胞上粘附分子的表达。已经发现了一个有趣的抗血管生成环,涉及IL-12、IFN-γ和CXC趋化因子配体10(CXCL10),并涉及CXCR4在增殖的血管内皮细胞上的表达。
IL-12在癌症免疫治疗方面的应用
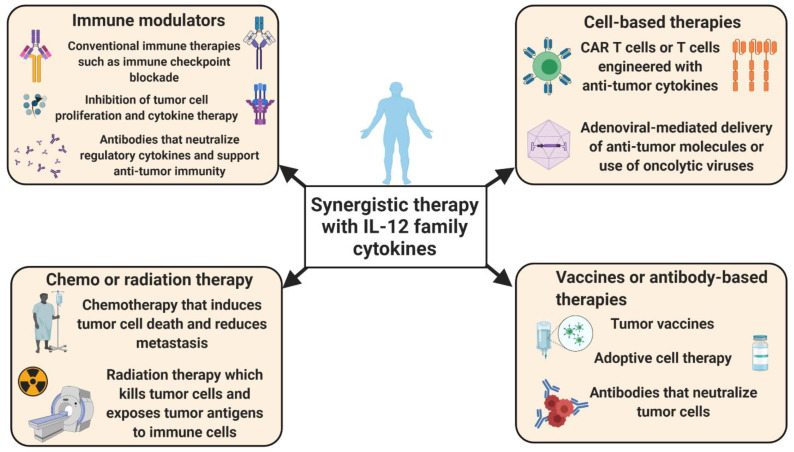
图 IL-12家族细胞因子的治疗性调节可以增强常规治疗的疗效
在临床前研究中,重组IL-12的全身给药在异种移植的小鼠模型中诱导了强大的抗肿瘤功效。然而,在临床试验中,重组蛋白在血清中的半衰期短,这意味着需要高剂量和多剂量,这导致了剂量相关的毒性,主要是由循环IFN-γ水平升高引起的。为了克服毒性,已经提出了不同的方法,重点通过局部递送IL-12以避免毒性全身暴露。几项临床前研究利用病毒载体、脂质体或体内电穿孔转染编码IL-12的质粒到可触及的肿瘤病变的局部区域,结果证实了其强大的抗肿瘤活性,且没有明显的毒性。专注于靶向蛋白递送,包含单链IL-12的融合蛋白与细胞外双链DNA结合抗体(从而靶向肿瘤坏死区)偶联,在小鼠模型中显示出增强的抗肿瘤活性。
基于IL-12的局部治疗可以与过继性T细胞转移协同结合。关于这种方法,在小鼠模型中评估了转基因肿瘤特异性T细胞的使用,该细胞被改造为在TME中分泌IL-12以响应TCR介导的抗原刺激,并显示出非常有希望的疗效。然而,在随后的临床试验中,报告了过继转移的TIL在产生诱导性IL-12过程中的渗漏,导致了不可接受的毒性,其中一例死亡。
局部IL-12递送和免疫刺激性单克隆抗体的使用可以产生协同结果。与此相一致,在临床前模型中,将IL-12的局部递送与PD-1–PD-L1的阻断相结合已被证明可以根除已建立的大型肿瘤。一种用体内电穿孔方法将IL-12作为单一药物(NCT01579318、NCT01502293和NCT02345330)和与pembrolizumab(NTC03132675)联合局部递送的临床试验也在进行中。
正如当前免疫肿瘤学临床试验的情况所示,联合方法似乎是加速临床影响的最有效方法。几种有前景的局部IL-12临床前联合方法可能在不久的将来被转化。人们对寻找能够增强淋巴细胞浸润的免疫调节剂以提高免疫检查点抑制剂的疗效产生了浓厚的兴趣。局部IL-12递送基于其驱动Th1反应、增强细胞溶解活性、保护T细胞免受PD-1/PD-L1耗竭和IFNγ诱导的细胞凋亡的能力,可能是免疫检查点抑制剂的理想伴侣。
如果安全性问题得到缓解,局部IL-12递送可用于早期癌症患者作为切除术的新辅助。对于无法手术的肿瘤,将局部IL-12递送与肿瘤消融技术相结合可能有助于增加局部和远处肿瘤的控制。随着有趣的组合方法,以及临床试验中基于IL-12的免疫疗法的增加,有理由相信局部IL-12递送可能在不久的将来在癌症免疫疗法中发挥重要作用。
产品推荐
| 货号 | 产品名称 | 规格 |
| CM014-5HP | Recombinant IL-12 p35,Human,AF | 5 μg |
| CM014-20HP | Recombinant IL-12 p35,Human,AF | 20 μg |
| CM014-100HP | Recombinant IL-12 p35,Human,AF | 100 μg |
| CM014-500HP | Recombinant IL-12 p35,Human,AF | 500 μg |
| CM014-1000HP | Recombinant IL-12 p35,Human,AF | 1 mg |
| CM160-5HP | Recombinant IL-12 p40,Human,AF | 5 μg |
| CM160-20HP | Recombinant IL-12 p40,Human,AF | 20 μg |
| CM160-100HP | Recombinant IL-12 p40,Human,AF | 100 μg |
| CM160-500HP | Recombinant IL-12 p40,Human,AF | 500 μg |
| CM160-1000HP | Recombinant IL-12 p40,Human,AF | 1 mg |
| CM182-5HP | Recombinant IL-12 p70 ,Human,AF,HEK293 | 5 μg |
| CM182-20HP | Recombinant IL-12 p70 ,Human,AF,HEK293 | 20 μg |
| CM182-100HP | Recombinant IL-12 p70 ,Human,AF,HEK293 | 100 μg |
| CM182-500HP | Recombinant IL-12 p70 ,Human,AF,HEK293 | 500 μg |
| CM182-1000HP | Recombinant IL-12 p70 ,Human,AF,HEK293 | 1 mg |
| CM011-5MP | Recombinant IL-12 p35,Mouse,AF | 5 μg |
| CM011-20MP | Recombinant IL-12 p35,Mouse,AF | 20 μg |
| CM011-100MP | Recombinant IL-12 p35,Mouse,AF | 100 μg |
| CM011-500MP | Recombinant IL-12 p35,Mouse,AF | 500 μg |
| CM011-1000MP | Recombinant IL-12 p35,Mouse,AF | 1 mg |
| CM012-5MP | Recombinant IL-12 p40,Mouse,AF | 5 μg |
| CM012-20MP | Recombinant IL-12 p40,Mouse,AF | 20 μg |
| CM012-100MP | Recombinant IL-12 p40,Mouse,AF | 100 μg |
| CM012-500MP | Recombinant IL-12 p40,Mouse,AF | 500 μg |
| CM012-1000MP | Recombinant IL-12 p40,Mouse,AF | 1 mg |
参考文献
· IL-12 Family Cytokines in Cancer and Immunotherapy. Cancers (Basel). 2021 Jan 6;13(2):167.
· Cytokines in clinical cancer immunotherapy.Br J Cancer. 2019 Jan;120(1):6-15.
· Localized Interleukin-12 for Cancer Immunotherapy. Front Immunol. 2020 Oct 15:11:575597.
· Regulatable interleukin-12 gene therapy in patie.nts with recurrent high-grade glioma: Results of a phase 1 trial.Sci Transl Med. 2019 Aug 14;11(505):eaaw5680.
· Advances in interleukin-12 gene therapy for acquired liver diseases. Curr Gene Ther. 2009 Apr;9(2):62-71.
· Regulation of the interleukin(IL)-12R beta 2 subunit expression in developing T helper 1 (Th1) and Th2 cells.J Exp Med. 1997 Mar 3;185(5):817-24.
· Leonard, J. P. et al. Effects of single-dose interleukin-12 exposure on interleukin-12-associated toxicity and interferon-gamma production.Blood. 1997 Oct 1;90(7):2541-8.
· Virotherapy with a Semliki Forest virus-based vector encoding IL12 synergizes with PD-1/PD-L1 blockade. Cancer Immunol Res . 2015 May;3(5):449-54.
· Lucas, M. L., Heller, L., Coppola, D. & Heller, R. IL-12 plasmid delivery by in vivo electroporation for the successful treatment of established subcutaneous B16.F10 melanoma.Mol Ther. 2002 Jun;5(6):668-75.
· The Immunobiology of the Interleukin-12 Family: Room for Discovery. Immunity. 2019 Apr 16;50(4):851-870.
· Tumor-infiltrating lymphocytes genetically engineered with an inducible gene encoding interleukin-12 for the immunotherapy of metastatic melanoma.Clin Cancer Res. 2015 May 15;21(10):2278-88.